Ученые из Центра исследований молекулярных механизмов старения и возрастных заболеваний МФТИ и Института биоорганической химии им. М. М. Шемякина и Ю. А. Овчинникова РАН с коллегами представили метод получения и очистки трансмембранного домена шиповидного белка коронавируса SARS-CoV-2 (SARStm) дикого типа. Этот «якорь» не только удерживает шип, которым вирус «атакует» клетки, в его оболочке, но и участвует в процессе слияния вирусной и клеточной оболочек.
В новом протоколе используется бесклеточная экспрессия — синтез белка в очищенном бактериальном экстракте, что позволяет получать его в течение нескольких часов вместо дней и значительно упрощает очистку. Метод открывает возможность для детального изучения структуры белка с помощью спектроскопии ядерного магнитного резонанса (ЯМР).
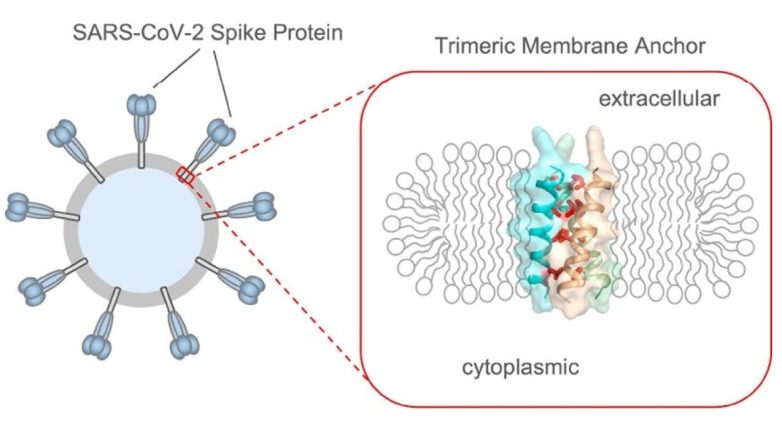
Трансмембранный домен — фрагмент шиповидного белка коронавируса — состоит из трех молекул, образующих единый большой комплекс, при этом в мембрану вируса погружена лишь маленькая его часть / © A Trimeric Hydrophobic Zipper Mediates the Intramembrane Assembly of SARS-CoV-2 Spike, Qingshan Fu and James J. Chou, Journal of the American Chemical Society
Несмотря на то что вирус SARS-CoV-2, вызывающий COVID-19, получил статус наиболее изученного вируса, пока нет полной ясности, как он проникает в клетку-хозяина. Известно, что в процессе заражения активно участвует шиповидный белок коронавируса (спайковый белок), но при этом его трансмембранный домен — фрагмент, пронизывающий оболочку вируса, — остается сравнительно мало изучен.
Изучение ТМД осложняется наличием в его первичной структуре (последовательности аминокислотных остатков, соединённых в цепочку) цистеинов, которые очень любят вступать в реакции. Из-за этого молекулы белка сшиваются друг с другом (образуют дисульфидные мостики) и выпадают в осадок, мешая эксперименту. Раньше эту проблему решали радикально: чтобы избежать слипания, первичную структуру белка намеренно изменяли (вводили мутации). Однако российские ученые из МФТИ с коллегами применили более тонкий подход. Они оставили первичную структуру «дикого типа» (природную), не заменяя цистеины на другие аминокислоты, как делали в других исследованиях. Вместо этого они взяли под контроль химические процессы, «размыкая» лишние связи и сохраняя структуру белка в целости для дальнейших исследований. Исследование опубликовано в журнале Biochemistry (Moscow), Supplement Series A: Membrane and Cell Biology.
Для осуществления цели российские ученые применили необычный метод синтеза белка, который вдобавок упростил его очистку. В предыдущих исследованиях белок получали с помощью живых клеток (стандартной бактериальной экспрессионной системы), поэтому приходилось использовать сложные многоступенчатые методы очистки, что могло непосредственно повлиять на то, каким образом белок собирается в тример. Чтобы избежать этого, биофизики из МФТИ с коллегами синтезировали белок SARStm без мутаций методом бесклеточной экспрессии, добавляя генетический материал (плазмиды) непосредственно в готовый экстракт бактерий, содержащий все компоненты для сборки белка. Новый подход позволил получить целевой белок быстрее, чем при производстве живыми клетками, и минимизировать этапы очистки.
Еще один плюс бесклеточной экспрессии — сборка белка напрямую из «изотопно-меченых» аминокислот. Они отличаются тем, что в составе аминокислот обычные атомы углерода и азота (¹²C и ¹⁴N) заменены на более тяжелые изотопы (¹³C и ¹⁵N). Благодаря «лишнему» нейтрону ядра приобретают магнитный момент и становятся «видны» в ходе исследования методом спектроскопии ядерного магнитного резонанса (ЯМР). Система меток позволяет восстановить структуру белка с высокой точностью. Чтобы получить меченый белок с помощью живых бактерий, их приходится растить на питательных средах с добавлением изотопно-меченых глюкозы и аммиака, что выходит дороже.
«Главной целью нашей работы было попробовать подобрать условия экспрессии и очистки белка дикого типа, то есть с его природной аминокислотной последовательностью без каких-либо изменений, — объяснила Софья Сударева, младший научный сотрудник лаборатории старения и возрастных нейродегенеративных заболеваний Центра исследований молекулярных механизмов старения и возрастных заболеваний МФТИ. — Стандартно после экспрессии мы растворяем белок в мицеллах ионного детергента — лауроилсаркозината (LS). Сложность оказалась в том, что в эти мицеллы даже при серьезном нагреве до +95૦С до белка не добирался β-меркаптоэтанол, который должен был разомкнуть цистеиновые мостики, что подняло бы белок из осадка. А помогла долгая выдержка при температуре +4૦С, что довольно неожиданно».
После очистки белка в мицеллах лауроилсаркозината (LS) от примесей ученые специально разрушили эти мицеллы, чтобы освободить и выделить чистый белок. В результате был получен изотопно-меченый белок ¹³C/¹⁵N SARStm высокой чистоты. Его выход составил 0,3 мг из 1 мл реакционной смеси — не максимальное, но достаточное количество для последующего анализа. Затем его переупаковали в новые мицеллы додецилфосфохолина. Эти мицеллы создают внутри себя среду, похожую на жировой слой клеточной мембраны, что позволяет гидрофобному белку принять правильную, рабочую форму и подготовить его для изучения методом ЯМР. ЯМР-анализ очищенного белка подтвердил его пригодность для дальнейших структурных исследований.
Разработанный протокол представляет собой более доступную и быструю альтернативу традиционным методам наработки белка для исследований. Он позволяет не только обойтись без дорогого культивирования бактерий на меченых средах, используя напрямую меченые аминокислоты, но и работать с «капризными» белками. Дальнейшая работа будет направлена на увеличение выхода целевого белка, вычисление его трехмерной структуры и определения механизма проникновения вируса в клетку с помощью этого «якоря».