В лаборатории впервые воссоздана нервная цепь человеческой боли
Ученые из Стэнфордского университета воспроизвели в лаборатории один из самых важных нервных путей, благодаря которому человек чувствует боль. Эта нервная цепь передает ощущения от кожи тела в мозг. Это достижение обещает ускорить медленный прогресс в понимании того, как обрабатываются болевые сигналы в организме человека и как лучше всего облегчить боль.
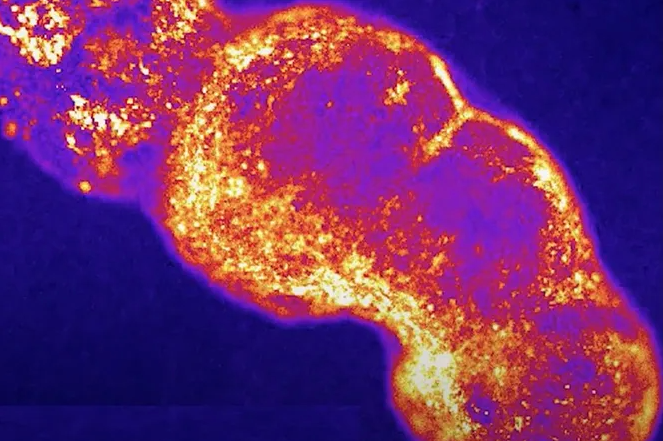
Выращенный в лаборатории нейронный путь.
Сегодня самые эффективные обезболивающие — это опиоидные препараты, которые имеют серьезный недостаток: они вызывают привыкание, что делает людей, страдающих от хронической боли, подверженными наркотической зависимости. Нужны другие средства, и чтобы их найти ученые воссоздали в лаборатории весь нейронный путь, по которому болевой сигнал приход в мозг.
Ученые из Стэнфордского университета воспроизвели в лаборатории один из самых важных нервных путей, благодаря которому человек чувствует боль. Эта нервная цепь передает ощущения от кожи тела в мозг. Это достижение обещает ускорить медленный прогресс в понимании того, как обрабатываются болевые сигналы в организме человека и как лучше всего облегчить боль. Работа опубликована в журнале Nature.
Периферическое ощущение боли передается в мозг по эстафете с участием нервных клеток, или нейронов, расположенных в четырех различных областях восходящего сенсорного пути: от корешковых ганглий к спинному мозгу, по которому сигнал поступает в регион головного мозга — таламус и дальше в соматосенсорную кору.
«Теперь мы можем моделировать этот путь не делая больно человеку», — говорит доктор Серджиу Паска, старший автор исследования. — «Мы надеемся, что это поможет нам узнать, как лучше лечить болевые расстройства».
До сих пор никто не мог наблюдать, как болевой сигнал передается по всему этому пути. Теперь Паска и его коллеги наблюдали волны электрической активности, идущие от первого компонента их конструкции до последнего, и смогли усилить или нарушить эти волнообразные паттерны путем изменения генов или химической стимуляции элементов цепи.
«Боль — это огромная проблема», — говорит врач Вивианна Тауфик, не принимавшая участия в работе. Но методы лечения боли немногочисленны и далеки от идеала, говорит Тауфик: «Я даже не могу передать, как грустно сидеть перед пациентом, страдающим от хронической боли, после того как вы перепробовали все, и в вашем арсенале ничего не осталось».
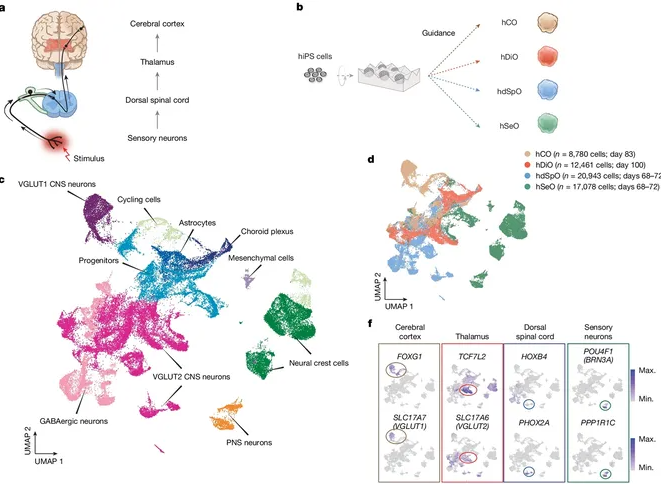
a, Схема, иллюстрирующая ключевые компоненты восходящего переднелатерального сенсорного пути. b, Схема, иллюстрирующая получение hCO, hDiO, hdSpO и hSeO из клеток hiPS. c, UMAP-визуализация экспрессии генов одной клетки hCO (день 83; n = 8 780 клеток из двух линий клеток hiPS13), hDiO (день 100; n = 12 461 клетка из трех линий клеток hiPS11), hdSpO (дни 68-72; n = 20 943 клетки из пяти линий клеток hiPS) и hSeO (дни 68-72; n = 17 078 клеток из четырех линий клеток hiPS). d, График UMAP, окрашенный в соответствии с идентичностью органоида. e, Состав клеток в каждом регионарном нейроорганоиде на основе данных scRNA-seq. f, Уровень экспрессии генов для маркеров региональной идентичности. g, Иммуноокрашивание для специфических региональных маркеров в hCO, hDiO, hdSpO и hSeO на 63-й день. h, Схема, иллюстрирующая создание атласа scRNA-seq DRG человека.
Регионы, составляющие восходящий сенсорный путь боли, связаны тремя наборами нейронных связей: первый набор передает сенсорную информацию от кожи через дорсальный корешковый ганглий в спинной мозг; второй набор нейронов передает сигналы от спинного мозга в мозговую структуру, называемую таламусом; а третий передает эту информацию от таламуса в соматосенсорную кору для дальнейшей обработки сигнала.
В новом исследовании Паска и его коллеги разработали человеческие органоиды, повторяющие четыре ключевые области восходящего сенсорного пути, а затем последовательно слили их вместе, чтобы сформировать ассемблоид, имитирующий весь путь.
Начав с клеток из образцов кожи добровольцев, команда сначала преобразовала их в индуцированные плюрипотентные стволовые клетки, которые по сути являются недифференцированными клетками, которые можно направить, чтобы они стали практически любым типом клеток в организме человека. Исследователи использовали химические сигналы, чтобы заставить эти клетки объединиться в крошечные шарики, называемые нейронными органоидами, представляющие каждую из четырех областей болевого пути.
Каждый органоид был немного меньше 3 мм в диаметре и содержал около миллиона клеток. Паска и его коллеги выстроили органоиды этих четырех разных типов бок о бок и стали ждать. Примерно через 100 дней они слились в ассемблоид длиной около 10 мм. «Они похожи на крошечные звенья сосиски», — говорит Паска, — «И состоят почти из 4 миллионов клеток. Это гораздо меньше, чем клеток в нервной системы, Но конструкция воспроизводит схему передачи болевого сигнала».
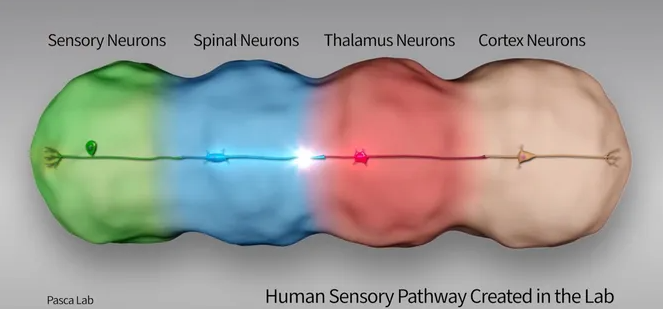
Нейронный болевой сигнал идет по ассемблоиду.
Исследователи показали, что все четыре органоида анатомически связаны: нейроны из первого образовали рабочие связи с нейронами из второго, второго с третьим, а третьего с четвертым.
И вся схема от сенсорного органоида, получающего сигнал, до органоида коры заработала как единое целое. После того, как все четыре органоида находились рядом друг с другом в колбе около 100 дней, начали проявляться паттерны спонтанной, синхронизированной сигнализации внутри ассемблоида: нейронная активность в сенсорном органоиде запускала действие в спинальном органоиде, затем в таламическом и, наконец, в корковом органоиде.
«Вы бы никогда не смогли увидеть эту волнообразную синхронность, если бы не могли наблюдать за всеми четырьмя органоидами, соединенными одновременно», — сказал Паска. «Мозг — это больше, чем сумма его частей».
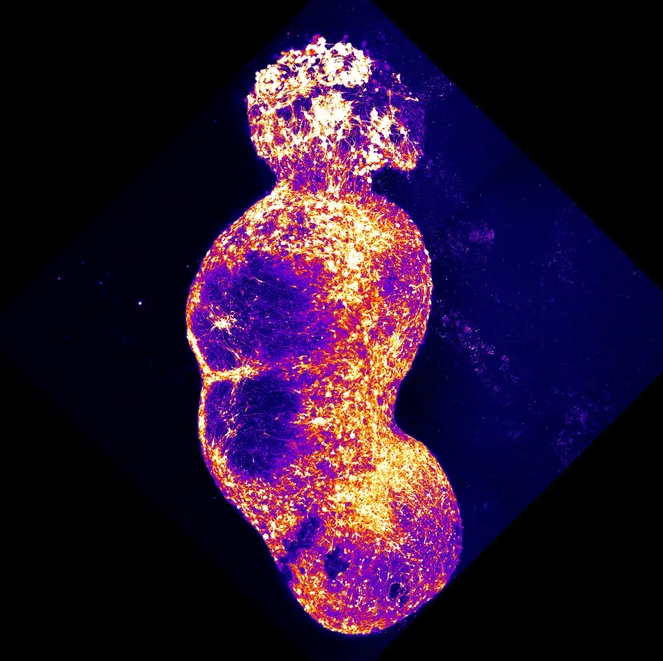
Исследователи создали ассемблоид, объединив четыре органоида, которые представляют четыре компонента сенсорного пути человека.
Химические вещества, известные тем, что вызывают боль, усиливают волнообразную активность в ассемблеоидах. Стимуляция сенсорного органоида капсаицином — ингредиентом перца чили, который вызывает жжение во рту — немедленно запускает волны нейронной активности.
Редкие генетические мутации в ионообменном белке Nav1.7, обнаруженном на поверхности периферических сенсорных нейронов, могут привести к изнурительной гиперчувствительности к боли или, наоборот, опасной для жизни неспособности испытывать боль — радикально увеличивая физические опасности, которые преподносит жизнь. Это ученые уже увидели, и это самое начало экспериментального исследования боли.
«Сами ассемблоиды не «чувствуют» никакой боли», — сказал Паска. — «Они передают нервные сигналы, которые должны быть дополнительно обработаны другими центрами в нашем мозге, чтобы мы могли испытать боль».
Ассемблоиды через несколько месяцев после их сборки представляют собой раннюю фазу развития плода, говорит Паска. Их непосредственное использование может помочь в изучении нарушений развития нервной системы, таких как аутизм. Люди с аутизмом часто гиперчувствительны к боли и сенсорной стимуляции в целом, и некоторые гены, связанные с аутизмом, активны в сенсорных нейронах восходящего болевого пути.
Паска сказал, что его лаборатория работает над способами ускорения развития ассемблеидов, чтобы лучше понять, как болевой путь работает (или не работает) у взрослых.
Паска говорит: «Мы считаем, что скрининг препаратов, которые подавляют способность сенсорных органоидов передавать сигнал, но при этом не влияют на систему вознаграждения мозга, как опиоиды (именно поэтому они вызывают привыкание), может привести к созданию новой целенаправленной терапии боли».

Выращенный в лаборатории нейронный путь.
Сегодня самые эффективные обезболивающие — это опиоидные препараты, которые имеют серьезный недостаток: они вызывают привыкание, что делает людей, страдающих от хронической боли, подверженными наркотической зависимости. Нужны другие средства, и чтобы их найти ученые воссоздали в лаборатории весь нейронный путь, по которому болевой сигнал приход в мозг.
Ученые из Стэнфордского университета воспроизвели в лаборатории один из самых важных нервных путей, благодаря которому человек чувствует боль. Эта нервная цепь передает ощущения от кожи тела в мозг. Это достижение обещает ускорить медленный прогресс в понимании того, как обрабатываются болевые сигналы в организме человека и как лучше всего облегчить боль. Работа опубликована в журнале Nature.
Периферическое ощущение боли передается в мозг по эстафете с участием нервных клеток, или нейронов, расположенных в четырех различных областях восходящего сенсорного пути: от корешковых ганглий к спинному мозгу, по которому сигнал поступает в регион головного мозга — таламус и дальше в соматосенсорную кору.
«Теперь мы можем моделировать этот путь не делая больно человеку», — говорит доктор Серджиу Паска, старший автор исследования. — «Мы надеемся, что это поможет нам узнать, как лучше лечить болевые расстройства».
До сих пор никто не мог наблюдать, как болевой сигнал передается по всему этому пути. Теперь Паска и его коллеги наблюдали волны электрической активности, идущие от первого компонента их конструкции до последнего, и смогли усилить или нарушить эти волнообразные паттерны путем изменения генов или химической стимуляции элементов цепи.
«Боль — это огромная проблема», — говорит врач Вивианна Тауфик, не принимавшая участия в работе. Но методы лечения боли немногочисленны и далеки от идеала, говорит Тауфик: «Я даже не могу передать, как грустно сидеть перед пациентом, страдающим от хронической боли, после того как вы перепробовали все, и в вашем арсенале ничего не осталось».
Создание сенсорного пути по частям

a, Схема, иллюстрирующая ключевые компоненты восходящего переднелатерального сенсорного пути. b, Схема, иллюстрирующая получение hCO, hDiO, hdSpO и hSeO из клеток hiPS. c, UMAP-визуализация экспрессии генов одной клетки hCO (день 83; n = 8 780 клеток из двух линий клеток hiPS13), hDiO (день 100; n = 12 461 клетка из трех линий клеток hiPS11), hdSpO (дни 68-72; n = 20 943 клетки из пяти линий клеток hiPS) и hSeO (дни 68-72; n = 17 078 клеток из четырех линий клеток hiPS). d, График UMAP, окрашенный в соответствии с идентичностью органоида. e, Состав клеток в каждом регионарном нейроорганоиде на основе данных scRNA-seq. f, Уровень экспрессии генов для маркеров региональной идентичности. g, Иммуноокрашивание для специфических региональных маркеров в hCO, hDiO, hdSpO и hSeO на 63-й день. h, Схема, иллюстрирующая создание атласа scRNA-seq DRG человека.
Регионы, составляющие восходящий сенсорный путь боли, связаны тремя наборами нейронных связей: первый набор передает сенсорную информацию от кожи через дорсальный корешковый ганглий в спинной мозг; второй набор нейронов передает сигналы от спинного мозга в мозговую структуру, называемую таламусом; а третий передает эту информацию от таламуса в соматосенсорную кору для дальнейшей обработки сигнала.
В новом исследовании Паска и его коллеги разработали человеческие органоиды, повторяющие четыре ключевые области восходящего сенсорного пути, а затем последовательно слили их вместе, чтобы сформировать ассемблоид, имитирующий весь путь.
Начав с клеток из образцов кожи добровольцев, команда сначала преобразовала их в индуцированные плюрипотентные стволовые клетки, которые по сути являются недифференцированными клетками, которые можно направить, чтобы они стали практически любым типом клеток в организме человека. Исследователи использовали химические сигналы, чтобы заставить эти клетки объединиться в крошечные шарики, называемые нейронными органоидами, представляющие каждую из четырех областей болевого пути.
Каждый органоид был немного меньше 3 мм в диаметре и содержал около миллиона клеток. Паска и его коллеги выстроили органоиды этих четырех разных типов бок о бок и стали ждать. Примерно через 100 дней они слились в ассемблоид длиной около 10 мм. «Они похожи на крошечные звенья сосиски», — говорит Паска, — «И состоят почти из 4 миллионов клеток. Это гораздо меньше, чем клеток в нервной системы, Но конструкция воспроизводит схему передачи болевого сигнала».

Нейронный болевой сигнал идет по ассемблоиду.
Исследователи показали, что все четыре органоида анатомически связаны: нейроны из первого образовали рабочие связи с нейронами из второго, второго с третьим, а третьего с четвертым.
И вся схема от сенсорного органоида, получающего сигнал, до органоида коры заработала как единое целое. После того, как все четыре органоида находились рядом друг с другом в колбе около 100 дней, начали проявляться паттерны спонтанной, синхронизированной сигнализации внутри ассемблоида: нейронная активность в сенсорном органоиде запускала действие в спинальном органоиде, затем в таламическом и, наконец, в корковом органоиде.
«Вы бы никогда не смогли увидеть эту волнообразную синхронность, если бы не могли наблюдать за всеми четырьмя органоидами, соединенными одновременно», — сказал Паска. «Мозг — это больше, чем сумма его частей».
Лечение боли без опиоидов

Исследователи создали ассемблоид, объединив четыре органоида, которые представляют четыре компонента сенсорного пути человека.
Химические вещества, известные тем, что вызывают боль, усиливают волнообразную активность в ассемблеоидах. Стимуляция сенсорного органоида капсаицином — ингредиентом перца чили, который вызывает жжение во рту — немедленно запускает волны нейронной активности.
Редкие генетические мутации в ионообменном белке Nav1.7, обнаруженном на поверхности периферических сенсорных нейронов, могут привести к изнурительной гиперчувствительности к боли или, наоборот, опасной для жизни неспособности испытывать боль — радикально увеличивая физические опасности, которые преподносит жизнь. Это ученые уже увидели, и это самое начало экспериментального исследования боли.
«Сами ассемблоиды не «чувствуют» никакой боли», — сказал Паска. — «Они передают нервные сигналы, которые должны быть дополнительно обработаны другими центрами в нашем мозге, чтобы мы могли испытать боль».
Ассемблоиды через несколько месяцев после их сборки представляют собой раннюю фазу развития плода, говорит Паска. Их непосредственное использование может помочь в изучении нарушений развития нервной системы, таких как аутизм. Люди с аутизмом часто гиперчувствительны к боли и сенсорной стимуляции в целом, и некоторые гены, связанные с аутизмом, активны в сенсорных нейронах восходящего болевого пути.
Паска сказал, что его лаборатория работает над способами ускорения развития ассемблеидов, чтобы лучше понять, как болевой путь работает (или не работает) у взрослых.
Паска говорит: «Мы считаем, что скрининг препаратов, которые подавляют способность сенсорных органоидов передавать сигнал, но при этом не влияют на систему вознаграждения мозга, как опиоиды (именно поэтому они вызывают привыкание), может привести к созданию новой целенаправленной терапии боли».
Только зарегистрированные и авторизованные пользователи могут оставлять комментарии.