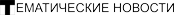Что предлагает наука людям с онкологией. Смелые разработки в лечении рака
Сегодня во всем мире онкологические заболевания остаются одной из главных проблем здравоохранения и ведущих причин смертности: по данным ВОЗ, с онкозаболеванием в течение жизни сталкивается примерно каждый пятый человек; каждый девятый мужчина и каждая двенадцатая женщина умирают от рака.
Число людей с диагнозом «рак» увеличивается ежегодно, на это влияют несколько факторов. С одной стороны, растет общая продолжительность жизни, а значит с возрастом увеличивается и шанс столкнуться с заболеванием, а с другой стороны, непрерывно совершенствуются методы диагностики, что повышает выявляемость опухолей, в том числе на ранних стадиях.
Не занимайтесь самолечением!
В наших статьях мы собираем последние научные данные и мнения авторитетных экспертов в области здоровья. Но помните: поставить диагноз и назначить лечение может только врач.
Ожидается, что в 2050 году людей с онкозаболеванием станет на 77% больше – около 35 млн пациентов по всему миру.
В этой ситуации медицина старается использовать все более эффективные методы лечения. А международное научное сообщество и инновационные фармкомпании предлагают смелые решения, которые в том числе позволяют полностью справиться с этим заболеванием.
О перспективных разработках, которые, возможно, в ближайшем будущем переведут онкозаболевания в разряд хронических болезней, во Всемирный день борьбы против рака редакции Techinsider.ru рассказала Мария Блохина, руководитель терапевтического направления отдела Онкология международной биофармацевтической компании AstraZeneca.
Наиболее перспективные решения можно условно разделить на три направления:
иммунотерапия;
таргетная терапия;
генная терапия.
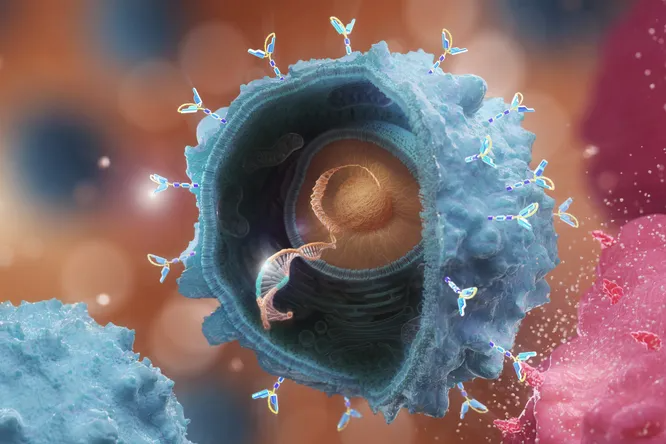
Но наука не стоит на месте и новым, перспективным направлением иммунотерапии, стала клеточная терапия, когда для уничтожения опухоли используются собственные клетки пациента: их учат распознавать и уничтожать рак.
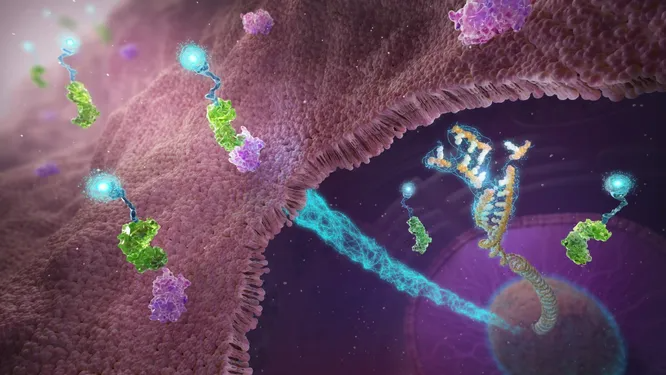
Сегодня разрабатывается несколько групп препаратов этого направления.
CAR-T терапия (химерные антигенные Т-клеточные рецепторы) — метод клеточной терапии, при котором собственные Т-лимфоциты (иммунные клетки) пациента модифицируются путем присоединения к ним искусственно созданного рецептора, нацеленного на уничтожение определенного типа опухолевых клеток.
Также перспективным направлением является клеточная терапия с использованием инженерного Т-клеточного рецептора (TCR-T). TCR-T способны распознавать большее количество антигенов опухолевой клетки, они способны связываться не только с антигенами на поверхности клетки, но и с внутриклеточными мишенями, включая опухоль-специфичные мутации.
Такие модифицированные клетки длительное время «живут» в организме пациента, активно выявляя и уничтожая клетки опухоли. Особенно эффективна клеточная терапия для наиболее тяжелых онкозаболеваний и их поздних стадий. Хотя потенциально клеточная терапия может продемонстрировать пользу и на ранних стадиях лечения онкозаболеваний. Известно, что сейчас разрабатываются решения, которые позволяют использовать разные популяции иммунных клеток и даже сделать универсальные клетки сразу для нескольких пациентов.
Пока сложный вопрос в разработке такой клеточной терапии — время производства препаратов. Для CAR-T это, как правило, несколько недель, что увеличивает время ожидания для пациентов зачастую с очень сложными состояниями.
Год назад AstraZeneca приобрела китайскую компанию Gracell Biotechnologies, специализирующуюся на CAR-T терапии. Разрабатываемая ими платформа FasTCAR значительно сокращает время производства клеточной терапии нового поколения с нескольких недель до нескольких дней и повышает пригодность T-клеток.
Применение клеточной терапии действительно может сделать прорыв в лечении рака, однако потребует от здравоохранения подготовленной инфраструктуры, которая позволит производить препарат из клеток пациента за очень короткий срок.
Таргетными препаратами могут быть различные классы веществ: малые молекулы, моноклональные антитела, а также конъюгаты моноклональных антител с химиотерапевтическими препаратами. Такие препараты способны доставлять мощный химиотерапевтический агент непосредственно к опухолевой клетке, прицельно уничтожая ее, но не затрагивая здоровые клетки. Такой механизм действия приводит к меньшему системному токсическому эффекту, при этом значимо увеличивает эффективность лечения.
Конъюгаты моноклональных антител уже сегодня используются, например, для помощи пациентам с различными опухолями, на поверхности опухолевых клеток которых имеется значительное количество рецептора HER2. Это могут быть рак молочной железы, немелкоклеточный рак легкого, опухоли желудочно-кишечного тракта или репродуктивной системы. Иногда стандартные варианты лечения у таких пациентов бывают неэффективными, тогда конъюгаты становятся терапией «спасения».
Но таргетно доставлять в опухоль можно не только молекулы химиотерапевтического препарата, но и источник ионизирующего излучения — радионуклид. Для этого создаются радиофармацевтические препараты — радиоконъюгаты, которые являются по сути молекулярно-направленной лучевой терапией. В настоящее время такие терапевтические препараты в рамках развития ядерной медицины разрабатываются для лечения различных типов опухолей.
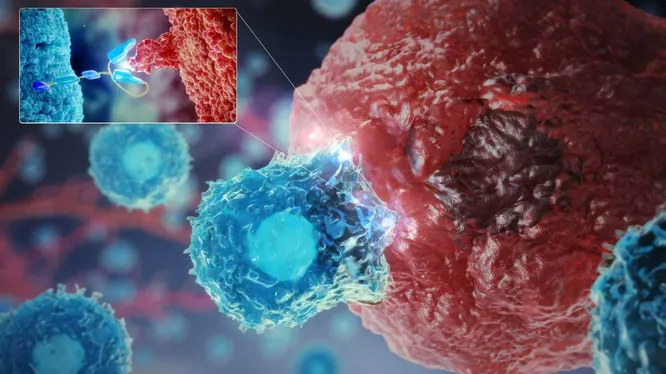
Редактирование генома, вероятно, в будущем сможет изменить подходы к лечению онкологических пациентов, воздействуя на наиболее фундаментальные механизмы возникновения и развития опухолевых клеток.
В условиях увеличения числа биомаркеров, которые нужно определить для выбора оптимальной лечебной стратегии, все более актуальными и доступными, становятся новые методы молекулярно-генетической диагностики, такие как секвенирование нового поколения, или NGS-тестирование. Этот метод наиболее чувствительный, то есть более точно определяет мутации, позволяет одновременно анализировать большое количество генов. При этом для анализа можно взять небольшой образец опухолевой ткани, а в ряде случаев может быть достаточно одной пробирки с кровью пациента.
NGS-тестирование будет эффективным как для выявления чувствительности опухоли к терапии, так и для определения наследственной предрасположенности к онкозаболеваниям.
Новые технологии используются для выявления патологии и врачами рентгенологами. Сегодня в России в диагностике, в том числе и онкологических заболеваний, рутинной практикой становится использование искусственного интеллекта.
И в контексте диагностики искусственный интеллект предоставляет много возможностей: он позволяет быстро обрабатывать массивы данных и уменьшает время анализа каждого отдельного исследования, снижает нагрузку на врача и делает исследования дешевле. Очевидно, это один из самых перспективных инструментов для выявления онкозаболеваний. И сегодня системы здравоохранения многих стран возлагают на него, как и на перспективные терапевтические разработки, большие надежды.

Число людей с диагнозом «рак» увеличивается ежегодно, на это влияют несколько факторов. С одной стороны, растет общая продолжительность жизни, а значит с возрастом увеличивается и шанс столкнуться с заболеванием, а с другой стороны, непрерывно совершенствуются методы диагностики, что повышает выявляемость опухолей, в том числе на ранних стадиях.
Не занимайтесь самолечением!
В наших статьях мы собираем последние научные данные и мнения авторитетных экспертов в области здоровья. Но помните: поставить диагноз и назначить лечение может только врач.
Ожидается, что в 2050 году людей с онкозаболеванием станет на 77% больше – около 35 млн пациентов по всему миру.
В этой ситуации медицина старается использовать все более эффективные методы лечения. А международное научное сообщество и инновационные фармкомпании предлагают смелые решения, которые в том числе позволяют полностью справиться с этим заболеванием.
О перспективных разработках, которые, возможно, в ближайшем будущем переведут онкозаболевания в разряд хронических болезней, во Всемирный день борьбы против рака редакции Techinsider.ru рассказала Мария Блохина, руководитель терапевтического направления отдела Онкология международной биофармацевтической компании AstraZeneca.
Индивидуальный подход к лечению рака
Максимальное количество прорывных решений сегодня сосредоточено в области персонализированной медицины. В ней фокус смещается с разработки препаратов на создание комплексных индивидуальных решений проблем конкретного пациента: диагностика, лечение, наблюдение в реальном времени.Наиболее перспективные решения можно условно разделить на три направления:
иммунотерапия;
таргетная терапия;
генная терапия.
Иммунная терапия
Суть иммунотерапии — в запуске процессов, которые позволяют собственной иммунной системе бороться с опухолевыми клетками. В настоящее время в практике онкологов уже применяются иммунотерапевтические препараты для лечения различных типов опухолей — так называемые блокаторы иммунных контрольных точек.Но наука не стоит на месте и новым, перспективным направлением иммунотерапии, стала клеточная терапия, когда для уничтожения опухоли используются собственные клетки пациента: их учат распознавать и уничтожать рак.

Сегодня разрабатывается несколько групп препаратов этого направления.
CAR-T терапия (химерные антигенные Т-клеточные рецепторы) — метод клеточной терапии, при котором собственные Т-лимфоциты (иммунные клетки) пациента модифицируются путем присоединения к ним искусственно созданного рецептора, нацеленного на уничтожение определенного типа опухолевых клеток.
Также перспективным направлением является клеточная терапия с использованием инженерного Т-клеточного рецептора (TCR-T). TCR-T способны распознавать большее количество антигенов опухолевой клетки, они способны связываться не только с антигенами на поверхности клетки, но и с внутриклеточными мишенями, включая опухоль-специфичные мутации.
Такие модифицированные клетки длительное время «живут» в организме пациента, активно выявляя и уничтожая клетки опухоли. Особенно эффективна клеточная терапия для наиболее тяжелых онкозаболеваний и их поздних стадий. Хотя потенциально клеточная терапия может продемонстрировать пользу и на ранних стадиях лечения онкозаболеваний. Известно, что сейчас разрабатываются решения, которые позволяют использовать разные популяции иммунных клеток и даже сделать универсальные клетки сразу для нескольких пациентов.
Пока сложный вопрос в разработке такой клеточной терапии — время производства препаратов. Для CAR-T это, как правило, несколько недель, что увеличивает время ожидания для пациентов зачастую с очень сложными состояниями.
Год назад AstraZeneca приобрела китайскую компанию Gracell Biotechnologies, специализирующуюся на CAR-T терапии. Разрабатываемая ими платформа FasTCAR значительно сокращает время производства клеточной терапии нового поколения с нескольких недель до нескольких дней и повышает пригодность T-клеток.
Применение клеточной терапии действительно может сделать прорыв в лечении рака, однако потребует от здравоохранения подготовленной инфраструктуры, которая позволит производить препарат из клеток пациента за очень короткий срок.
Таргетная терапия
Еще один современный метод лечения рака — таргетная терапия. Она уничтожает раковые клетки путем воздействия на мутацию или биомаркер, специфичный для опухолевых клеток, не затрагивая при этом здоровые ткани и органы. Это позволяет сделать лечение более эффективным, безопасным и менее токсичным. Это так называемая, «молекулярно-направленная терапия».Таргетными препаратами могут быть различные классы веществ: малые молекулы, моноклональные антитела, а также конъюгаты моноклональных антител с химиотерапевтическими препаратами. Такие препараты способны доставлять мощный химиотерапевтический агент непосредственно к опухолевой клетке, прицельно уничтожая ее, но не затрагивая здоровые клетки. Такой механизм действия приводит к меньшему системному токсическому эффекту, при этом значимо увеличивает эффективность лечения.
Конъюгаты моноклональных антител уже сегодня используются, например, для помощи пациентам с различными опухолями, на поверхности опухолевых клеток которых имеется значительное количество рецептора HER2. Это могут быть рак молочной железы, немелкоклеточный рак легкого, опухоли желудочно-кишечного тракта или репродуктивной системы. Иногда стандартные варианты лечения у таких пациентов бывают неэффективными, тогда конъюгаты становятся терапией «спасения».
Но таргетно доставлять в опухоль можно не только молекулы химиотерапевтического препарата, но и источник ионизирующего излучения — радионуклид. Для этого создаются радиофармацевтические препараты — радиоконъюгаты, которые являются по сути молекулярно-направленной лучевой терапией. В настоящее время такие терапевтические препараты в рамках развития ядерной медицины разрабатываются для лечения различных типов опухолей.
Генная терапия
Третье перспективное направление в лечении онкозаболеваний — генная терапия. Это метод, при котором вносятся изменения в генетический аппарат, чтобы вылечить заболевание. Понимая, что причина появление раковых клеток – это мутации в структуре ДНК, разработчики генной терапии используют здоровые гены для замены или исправления как раз тех дефектных генов в раковых клетках. При таком подходе последовательность генома напрямую изменяется путем добавления, замены или удаления оснований ДНК.
Редактирование генома, вероятно, в будущем сможет изменить подходы к лечению онкологических пациентов, воздействуя на наиболее фундаментальные механизмы возникновения и развития опухолевых клеток.
Успех лечения – за точной диагностикой
Персонализация терапии требует все более современных и точных подходов к диагностике. Сейчас все чаще совместно с таргетными препаратами регистрируются и диагностические решения для выявления той или иной мутации или биомаркера: они позволяют определить целевую популяцию пациентов для терапии, сократить время постановки диагноза и использовать более точечную стратегию лечения.В условиях увеличения числа биомаркеров, которые нужно определить для выбора оптимальной лечебной стратегии, все более актуальными и доступными, становятся новые методы молекулярно-генетической диагностики, такие как секвенирование нового поколения, или NGS-тестирование. Этот метод наиболее чувствительный, то есть более точно определяет мутации, позволяет одновременно анализировать большое количество генов. При этом для анализа можно взять небольшой образец опухолевой ткани, а в ряде случаев может быть достаточно одной пробирки с кровью пациента.
NGS-тестирование будет эффективным как для выявления чувствительности опухоли к терапии, так и для определения наследственной предрасположенности к онкозаболеваниям.
Новые технологии используются для выявления патологии и врачами рентгенологами. Сегодня в России в диагностике, в том числе и онкологических заболеваний, рутинной практикой становится использование искусственного интеллекта.
И в контексте диагностики искусственный интеллект предоставляет много возможностей: он позволяет быстро обрабатывать массивы данных и уменьшает время анализа каждого отдельного исследования, снижает нагрузку на врача и делает исследования дешевле. Очевидно, это один из самых перспективных инструментов для выявления онкозаболеваний. И сегодня системы здравоохранения многих стран возлагают на него, как и на перспективные терапевтические разработки, большие надежды.
Только зарегистрированные и авторизованные пользователи могут оставлять комментарии.